Apabila Suatu Unsur Melepas Elektron Maka – Suatu unsur dengan 2 elektron 6. Kecenderungan unsur tersebut ketika akan berikatan dengan unsur lain adalah A. Melepaskan 2 elektron menjadi muatan +2 B. Melepaskan 4 elektron menjadi muatan +4 C. Menggabungkan 4 elektronnya dengan 4 elektron lainnya D. Kehilangan 4 elektron bermuatan -4 E. Menyerap 2 elektron bermuatan -2
Suatu unsur dengan keelektronegatifan 2 6. Kecenderungan unsur ini berikatan dengan unsur lain adalah melepaskan 2 elektronnya sehingga bermuatan -2 (E).
Apabila Suatu Unsur Melepas Elektron Maka
Pada soal di atas, unsur memiliki konfigurasi elektron 2 6, sehingga unsur tersebut membutuhkan 2 elektron untuk mencapai kestabilan (aturan oktet) sehingga unsur tersebut harus
Kumpulan Contoh Soal Susunan Elektron Stabil
Pada soal di atas, unsur memiliki 2 6 pasangan elektron, sehingga unsur kehilangan 2 elektron untuk mencapai kestabilan (aturan oktet) sehingga unsur tersebut harus memperoleh 2 elektron untuk memiliki muatan -2.
Pertanyaan baru di Kimia, tolong jawab ya… pertanyaan1. Hewan laut yang punah adalah….. 2. Bahan bakar fosil berasal dari….. 3. hewan apa yang bereproduksi… secara ovovivipar? ok, itu saja untuk 100 poin, apa pertanyaan selanjutnya? Kuis sains dasar atom Ar H = 1, 0 = 16 Berapa massa 9 gram H2O pada suhu , 27°? c dan tekanan atom 2 Ar H = 1, 0 = 16 Jelaskan kegunaan minyak dan lemak serta ester lebih dari ikatan ionik Ikatan kovalen: ikatan kovalen rangkap/ganda ikatan kovalen polar ikatan kovalen nonpolar ikatan kovalen semipolar
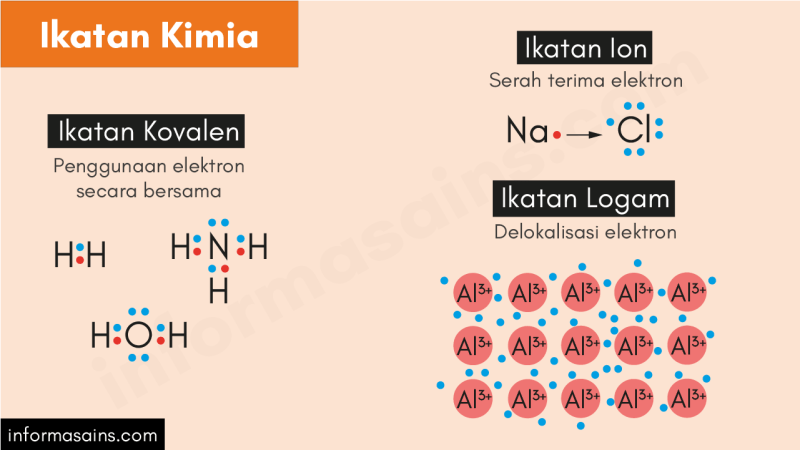
3 DEFINISI IKATAN KIMIA Ikatan kimia interaksi antar atom yang bergabung membentuk molekul, senyawa atau ion Reaksi kimia tarik menarik antar atom yang menimbulkan ikatan kimia
4 Bonding Bonding adalah interaksi elektronik antar atom secara bersama-sama membentuk molekul, partikel atau gugus atom untuk membentuk ikatan kimia mencapai stabilitas.
Solution: Sel Elektrolisis
Menurut Lewis (teori oktet) atom-atom unsur memiliki kecenderungan stabil sebagai gas ideal terdekat dengan orde 8e pada kulit terluar (oktet), kecuali helium yang memiliki 2e‑ pada kulit terluar (duplet). .
Simbol Atom Jumlah Elektron dalam Kulit Jumlah Elektron Valen K L M N O P 2He 2 10Ne 8 18Ar 36Kr 18 54Xe 86Rn 32
A. Pelucutan elektron Kecenderungan untuk melepaskan elektron ditemukan pada unsur logam dengan energi ionisasi rendah (yaitu, elektrostatis). Atom unsur logam cenderung kehilangan elektron valensi membentuk ion +x dengan x = jumlah gugus utama. Atom kehilangan elektron untuk memiliki 8 elektron valensi (oktet) atau memiliki 2 elektron valensi (duplet), seperti gas mulia (golongan VIIIA/gas inert).
Atom memperoleh elektron dalam golongan IVA, VA, VIA, VIIA Golongan IA elektron valensi = 1 kehilangan satu elektron, membentuk ion +1, yaitu: Li+, Na+, K+ Golongan IIA elektron valensi = 2 melepaskan elektron 2 ke membentuk ion +2 yaitu: Mg + 2, Ca + 2, Sr + 2, Ba + 2, Ra + 2
Soal Materi Sifat Keperiodikan Unsur 1.pdf
19K ( ) melepaskan 1 elektron K + ion: menurut struktur 18Ar 12Mg ( ) Mg2 + ion (2. 8) melepaskan 2 e 20Ca ( ) melepaskan 2 elektron ion Ca + 2: menurut strukturnya dari 18Ar
10b. Penangkapan Elektron Penangkapan elektron dicapai oleh non-logam karena mereka memiliki afinitas elektron yang tinggi (sifat elektronegatif). Atom menarik/mengikat elektron sehingga memiliki 8 (oktet) atau 2 (duplet) elektron valensi seperti gas mulia (gas inert/golongan VIIIA).
😯 (2.6) e ion O-2 (2.8) struktur Ne 16S (2.8.6) + 2 e ion S-2 (2.8.8) Ar struktur 7N (2.5) e ion N -3 (2. 8) bentuk Ne
12 NILAI NILAI Elektron valensi berperan dalam menciptakan ikatan antar atom dengan membentuk ikatan. Sebagian besar sifat kimia unsur ditentukan oleh elektron valensinya. Elektron valensi dalam atom diwakili oleh titik (.) atau tanda silang kecil (x) yang disebut struktur Lewis.
Modul Reaksi Redoks Kelas X Bermuatan Karakter Berbasis Guided Inquiry
Jenis ikatan kimia didasarkan pada bagaimana atom dari berbagai unsur distabilkan: Ikatan ionik Ikatan kovalen: Ikatan kovalen ganda (dua dan tiga) Ikatan kovalen kolom Ikatan kovalen polar
14 Ikatan Ion adalah ikatan kimia yang terjadi antara logam dan non logam dengan mendonorkan elektron valensi sehingga menghasilkan ion positif dan negatif yang berikatan dengan gaya elektrostatis Contoh : 1. Logam IA dan IIA (kecuali H dan Be) dan non logam VIA dan VIIA 2 Logam IA dan IIA (kecuali Be, Mg) dan H Contoh: Transformasi NaCl dari natrium dan klor dapat dijelaskan dengan rumus elektron (rumus Lewis) sebagai berikut:
Solusi: 19K = K + 😯 = 2.6 O2- K e + K + ) x2 2e + O O2- 2K + O 2K + + O2- K2O
17 Ikatan Kovalen Ikatan kovalen terbentuk dengan berbagi dua pasang elektron dari atom yang berikatan. Ikatan ini ada antara non-logam dan logam yang keduanya ingin menahan elektron. Contoh : Pada senyawa FCl Perhatikan elektron ikatan (bonding electron) antara F dan Cl. Kombinasi elektron dari F dan Cl. Pasangan elektron dibagi sehingga setelah menggabungkan elektron valensi dari dua atom “seolah-olah” menjadi 8 (oktet) seperti gas mulia.
Materi + Contoh Soal Ipa
Ikatan ini melibatkan penggunaan bersama lebih dari dua elektron oleh dua atom yang berikatan. Ikatan kovalen rangkap/ganda terbagi menjadi dua yaitu ikatan kovalen rangkap dua dan ikatan kovalen rangkap tiga.
A.1. Ikatan rangkap Contoh: Ikatan antara dua atom oksigen membentuk molekul O2 Contoh lain ikatan rangkap: CO2
Contoh: Ikatan antara atom oksigen dan atom nitrogen dalam molekul NTA. Ikatan rangkap tiga N2 (g) sangat kuat sehingga N2 sulit bereaksi di atmosfer. N2 adalah barang yang sangat serbaguna. N2 masuk dan keluar tubuh manusia tidak berubah secara kimiawi. Pada suhu dan tekanan tinggi N2 hanya dapat bereaksi terhadap perpecahan.
21 b. Ikatan Kovalen Polar Ketika dua atom (diatomik) yang berbeda bergabung bersama, molekul tersebut memiliki polaritas (positif dan negatif), yang disebut polar. Ini tergantung pada momen dipol. Posisi dipol adalah produk dari jarak ikatan antara atom yang terikat dan perbedaan keelektronegatifan antara dua atom yang terikat. Semakin besar posisi dipol, semakin polar kombinasinya. Senyawa dengan muatan nol (0) disebut senyawa non-polar. Molekul polar memiliki struktur (struktur) molekul yang unik: atom dengan elektronegativitas tinggi tidak berinteraksi dengan atom dengan elektronegativitas rendah. Jadi itu seperti molekul bermuatan.
Jika Unsur Unsur Berikut Membentuk Konfigurasi Elektron Stabil Seperti Unsur Gas Mulia, Tentukan
Senyawa poliatomik simetris yang atom pusatnya elektron bebas (lone electron) selalu polar memiliki PEB. Ini karena pasangan elektron bebas lebih kuat dari ikatan, menghasilkan elektronegativitas yang lebih besar. Selisih nilai keelektronegatifan ≤ 1,7 Contoh : H2O, NH3
Ciri-ciri senyawa kovalen non-polar: 1. Satu molekul diatomik selalu kovalen dan selalu non-polar. Ini karena elektron tertarik di kedua arah oleh gaya tarik-menarik (keelektronegatifan) yang sama. Contoh: H2, O2, F2 2. Molekul poliatomik simetris yang atom pusatnya tidak memiliki pasangan elektron bebas (lone electron) selalu nonpolar. Contoh: CCl4, CH4, CO2, SF6, PCl5
Ikatan Kovalen adalah ikatan kovalen yang terjadi ketika sebuah elektron dibagi dari salah satu atom ikatan, sedangkan atom lainnya tidak berkontribusi. Contoh: H3O+, N2O, SO2, SO3, H2SO4, NH4+
Agar situs web ini berfungsi, kami mengumpulkan data pengguna dan membagikannya dengan administrator kami. Untuk menggunakan situs ini, Anda harus menyetujui Kebijakan Privasi kami, termasuk kebijakan cookie kami. Pada tahun 1927, W. Heisenberg menetapkan Prinsip Ketidakpastian, yaitu posisi elektron di sekitar inti tidak dapat ditentukan secara tepat. Model mekanik atom menunjukkan bahwa elektron dalam atom menempati orbital, yaitu ruang atau awan di mana kemungkinan elektron ditemukan dalam atom tinggi.
Bab 1 Struktur Atom Dan Sistem Periodik Unsur Kata Kunci Pengantar Pages 1 44
Satu kulit terdiri dari banyak subkulit, satu subkulit terdiri dari orbital, sedangkan satu orbital berisi maksimal dua elektron.
Nyatakan posisi elektron dalam suatu orbital dengan menggunakan tiga bilangan, yaitu bilangan kuantum utama (n), bilangan azimuth (l), dan bilangan magnetik (m).
Bilangan pokok (n) menyatakan tingkat energi pokok atau kulit atom. Nilai numerik utama adalah bilangan bulat dari 1 hingga tak terhingga (1, 2, 3,…..).
Nomor medan magnet (m) menunjukkan orbital unik yang dibentuk oleh elektron di subkulit. Nilai medan magnet tergantung pada jumlah azimuth, yaitu –l,. . .0. . . ., +l.
Suatu Unsur Konfigurasi Elektronnya Adalah 2 6. Kecenderungan Unsur Tersebut Bila Akan Berikatan
Susunan elektron dalam subkulit atom disebut konfigurasi elektron. Ada tiga hukum yang digunakan untuk menulis diagram elektronik, yaitu prinsip Aufbau, prinsip eksklusi Pauli, dan aturan Hund.
Menurut hukum Aufbau, pengisian elektron dimulai dari subkulit energi yang lebih rendah ke tingkat energi yang lebih tinggi.
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f < 6d < 7p
Pengisian elektron pada orbital cenderung tidak terisi terlebih dahulu, kemudian bila tidak ada orbital lain yang kosong maka elektron tersebut akan berikatan.
Notasi Penulisan Partikel Sub Atom
₂₆L = 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶, disingkat golongan gas mulia (VIIIA), mendekati muatan elektron gas ₁₈Ar.
Masalah Baru dalam Kimia 1. Coba perhatikan syarat-syarat mengendarai sepeda suspensi. Mengapa ada batasan?
Apabila dalam membagikan masakan aqiqah sedangkan jumlah barang terbatas maka yang diutamakan adalah, konfigurasi elektron unsur, apabila kita akan menghapus database dalam mysql maka menggunakan perintah, apabila tubuh kekurangan zat besi maka dapat mengakibatkan penyakit, elektron valensi unsur, suatu integrasi sosial akan tercapai apabila, apabila kita kekurangan minum maka kita akan mengalami, unsur unsur berdirinya suatu negara, apabila bagian telinga nomor 4 berlubang maka, unsur terbentuknya suatu negara, apabila sel telur tidak dibuahi maka, konfigurasi elektron unsur transisi